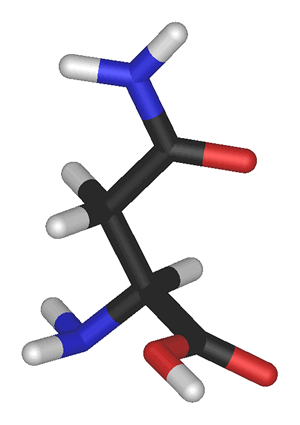
A asparagina é derivada do ácido aspártico. Participa na biossíntese de glicoproteínas e é essencial na síntese de um grande número de outras proteínas. É um dos aminoácidos codificados pelo código genético, sendo portanto um dos componentes das proteínas dos seres vivos.
A asparagina representa cerca de 3% dos aminoácidos das proteínas do organismo humano. Pode ser utilizada para normalizar as funções celulares do cérebro e do Sistema nervoso central (SNC).
Trata-se de um dos vinte aminoácidos mais comuns no planeta Terra. É um composto orgânico cuja fórmula química é NH2CH(NH2)COOH, possuindo uma carboxamida como grupo funcional da cadeia lateral.
A asparagina é um aminoácido que apresenta quiralidade – existem dois estereoisómeros: L-arginina e D-arginina.
Quando pura é um sólido cristalino branco inodoro. Enquanto a L-arginina não apresenta sabor, a D-arginina tem um sabor adocicado. É um composto estável, não inflamável e apresenta baixo risco para a saúde (é ligeiramente irritante).
A asparagina foi isolada pela primeira vez em 1806, sob a forma cristalina, pelos químicos franceses Louis Nicolas Vauquelin e Pierre Jean Robiquet, a partir do suco de espargos, nos quais este aminoácido é abundante (daí o nome asparagina), tendo sido o primeiro aminoácido a ser isolado.
A reação desta com açúcares redutores, ou grupos carbonilo reativos, produz acrilamida em alimentos quando aquecidos a altas temperaturas, tais como batatas fritas, pão torrado e outros produtos amiláceos sujeitos a fritura.
A asparagina é um aminoácido não-essencial, uma vez que pode ser sintetizado a partir de intermediários das vias metabólicas principais. Existe em lacticínios, aves, ovos, carne de vaca, peixe e marisco. Também se encontra presente em produtos vegetais, tais como espargos, batatas, nozes, sementes e leguminosas.
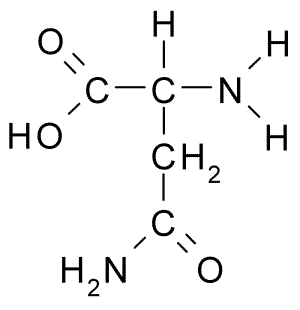
Nome sistemático (IUPAC): Ácido 2-aminossuccionâmico
Abreviatura/Símbolo: N / Asn
Fórmula química: C4H8N2O3
Massa Molecular: 132.1
Ponto de fusão: 234.5 °C
Imagem "Asparagina 3d". Licenciado sob CC BY-SA 3.0, via Wikimedia Commons