Existem três tipos de unidades estruturais que podem constituir a matéria. São elas os átomos, as moléculas e os iões.
Os iões são as únicas unidades estruturais da matéria que apresentam carga elétrica, isto é, não são neutros.
Os iões formam-se quando os átomos (ou algumas moléculas) sofrem um ganho ou uma perda de eletrões, de forma a que consigam ficar com uma maior estabilidade.
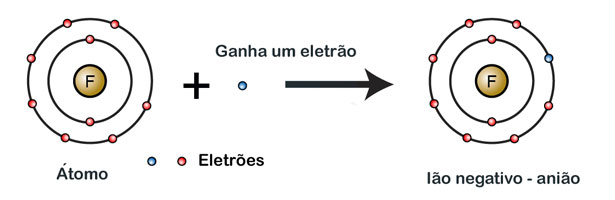
Na figura 1 pode observar-se um átomo de flúor (que possui nove protões e nove eletrões). É por isso uma partícula sem carga elétrica, ou neutra.
Repara que quando recebe um eletrão, a partícula resultante fica com os mesmos nove protões e dez eletrões. Por essa razão (o número de eletrões é maior que o número de protões) transforma-se num ião negativo ou anião, com uma carga negativa (-1).
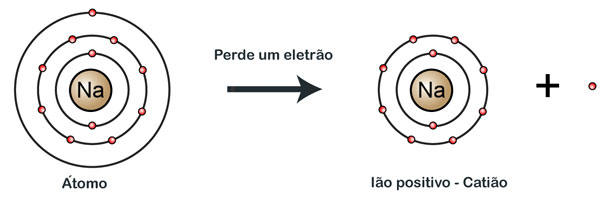
Vejamos agora o exemplo contrário:
|
Os iões negativos ou aniões formam-se quando um átomo ganha um ou mais eletrões. Os iões positivos ou catiões formam-se quando um átomo perde um ou mais eletrões. |
Apesar de existir alterações na carga elétrica da partícula, pois o número de eletrões é alterado (aumentando ou diminuindo), o número atómico do elemento que origina o ião não se altera.
|
O número de protões que estão no núcleo não se altera neste processo. Isso quer dizer que o número de protões é sempre o mesmo no átomo e no ião que se forma a partir desse átomo. A carga de um ião calcula-se subtraíndo ao número total de eletrões do átomo que o originou (ou grupo de átomos), o seu número de eletrões. |
Vamos ver então dois exemplos:
O ião cloreto quando se forma a partir do átomo de cloro, recebe um eletrão. O átomo de cloro possui 17 protões e 17 eletrões (por isso não tem carga elétrica, porque 17-17 = 0). O ião cloreto tem os mesmos 17 protões (porque o número de protões não se altera) e tem 18 eletrões (porque recebeu um).
A carga deste ião é -1 (17 eletrões do átomo menos 18 eletrões do ião).
O ião cálcio quando se forma perde dois eletrões. O átomo de cálcio tem 20 protões e 20 eletrões. O ião cálcio tem apenas 18 eletrões.
A carga do ião cálcio é +2 (20 - 18).
Podes consultar também:
Carga dos iões
1. Considera o ião que se forma a partir do átomo de sódio (Na) sabendo que o sódio perde um eletrão. O número atómico deste átomo é 11 e o seu número de massa 23.
1.1. Indica qual é a carga do ião formado.
1.2. Diz como é constituído o ião sódio.
1.1. Se o número atómico do sódio é 11, isso quer dizer que ele tem 11 protões. Como os átomos são neutros, terá também 11 eletrões. Se o ião sódio, quando se formou perdeu um eletrão, então ele ficou com 10 eletrões (11-1).
1.2. O ião sódio é constituído por: 11 protões, 10 eletrões e 12 neutrões (23-11).